Spørger du dine ældre patienter om naturmedicin?
Artikel fra Rationel Farmakoterapi 4, 2018
Månedsbladene opdateres ikke efter udgivelsen. Indholdet afspejler den aktuelle evidens på udgivelsestidspunktet.
- Stine Rasch: Hæmatologisk Afdeling, Sydvestjysk Sygehus, Esbjerg
- Zandra N. Ennis: Afdeling for Klinisk Biokemi og Farmakologi, Odense Universitetshospital
- Lars Peter Nielsen: Klinisk Farmakologisk Afdeling, Aarhus Universitetshospital
- Jens-Ulrik Rosholm: Geriatrisk afdeling, Odense Universitetshospital
I den vestlige verden er andelen af ældre i befolkningen stigende. Således forventes det, at andelen af danskere på 65-89 år vil være 39% større i 2060 sammenlignet med i dag [1].
I takt med, at mortaliteten falder, og befolkningen ældes, bliver multimorbiditet og polyfarmaci hyppigere blandt de ældre [2, 3]. Især polyfarmaci og et samtidigt forbrug af naturlægemidler gør denne patientgruppe sårbar i forhold til potentielle lægemiddelinteraktioner.
Definitioner
Naturmedicin
Betegnelsen naturmedicin bliver ofte brugt i flæng om mange typer af naturprodukter, som bruges til at forebygge eller behandle symptomer eller sygdomme, og kan dække over blandt andet naturlægemidler, stærke vitaminer og mineraler, traditionelle plantelægemidler samt homøopatiske lægemidler[4]. Naturmedicin er en del af begrebet CAM (Complementary and Alternative Medicine), som dækker over alle typer af alternativ behandling, som enten bruges sammen med eller erstatter konventionel medicin. I begrebet CAM indgår således alt fra naturmedicin, akupunktur og kiropraktik til healing og afslapningsterapi [5, 6].
Naturlægemidler
Naturlægemidler er en gruppe af lægemidler, hvis aktive indholdsstoffer udelukkende er naturligt forekommende stoffer af animalsk, vegetabilsk eller mineralsk oprindelse, og hvis koncentration ikke er væsentlig større end dem, hvori de forekommer i naturen [7]. Modsat kosttilskud, der hører under fødevarelovgivningen, er naturlægemidler omfattet af lægemiddellovgivningen, og produkterne må
derfor markedsføres som forebyggende eller helbredende på specifik sygdom eller sygdomssymptomer, så længe disse indikationer kun omfatter lettere sygdomme som f.eks. forstoppelse, slimløsende etc. Dette til anvendelse i en kortere periode, hvor det ikke er almindeligt at søge læge [7]. Der er dertil krav om, at produkterne skal være betryggende fremstillet og af tilfredsstillende kvalitet samt ved normal anvendelse være uskadelige og dokumenteret forsvarlige at anvende på anførte indikationer. Hvis bestanddelene i præparatet er almindelig anerkendte, er resultater af farmakologiske og toksikologiske undersøgelser eller kliniske studier ikke et krav [7]. Dette forhold medfører, at eventuelle interaktioner ofte ikke er velundersøgte. Som nævnt skelnes der i Danmark og andre nordiske lande ikke mellem, om de naturligt forekommende stoffer i et naturlægemiddel er af animalsk, vegetabilsk eller mineralsk oprindelse. Dette betyder, at fiskeolie, mælkesyreproducerende bakterier o.l. kan indgå i et naturlægemiddel. Disse forhold adskiller sig fra de øvrige lande i Europa, hvor naturlægemidler betegnes ”herbal medicinal products”, hvilket vil sige, at disse præparater alene er baseret på plantemateriale [7]. Desuden hersker der forskellige kulturer i forhold til brugen af naturmedicin i de vestlige europæiske lande. Eksempelvis er plantebaseret medicin i højere grad en del af den moderne medicin i Tyskland i forhold til Danmark.
I Tyskland er der 600-700 plantebasererede lægemidler, som udskrives af ca. 70% af landets læger [8].
Anvendelse af naturmedicin
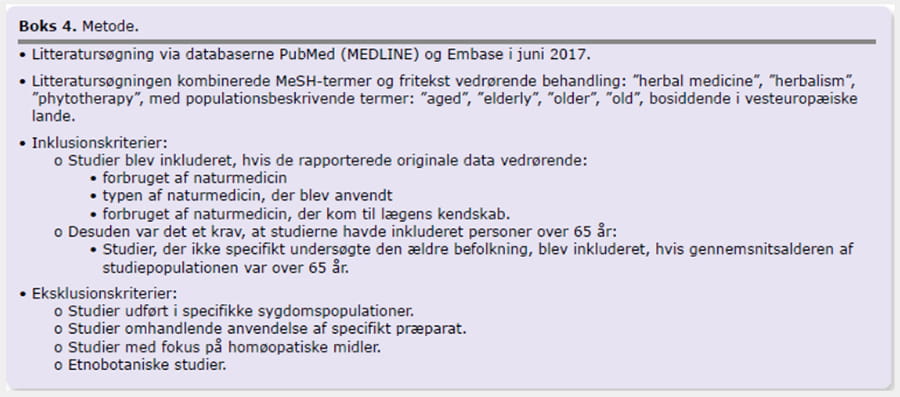
I denne artikel er forbruget af naturmedicin hos +65-årige i Vesteuropa undersøgt på baggrund af en systematisk litteratursøgning og gennemgang, hvori der indgik 17 studier.
Endvidere er det undersøgt, hvilke typer af naturmedicin der blev anvendt, og i hvor høj grad lægerne havde kendskab til forbruget. Herudover præsenteres en oversigt over hyppigt anvendte naturlægemidler, potentielle interaktioner og foreslåede tiltag.
Hvor mange anvender naturmedicin?
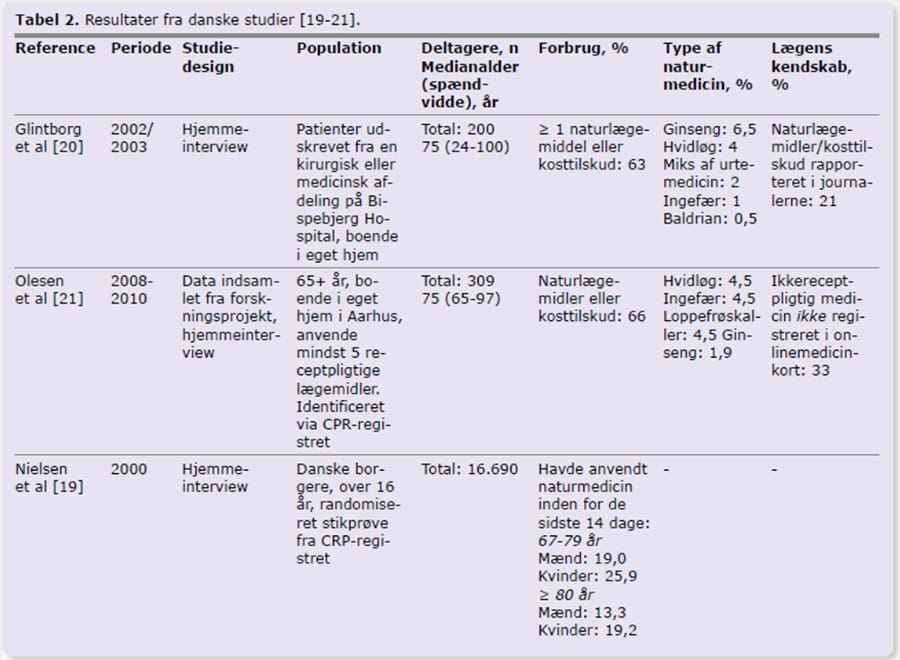
Andelen af ældre, der anvender naturmedicin i de europæiske lande, svinger meget. Således varierede andelen, der anvender naturmedicin, fra 2,7% til 63,9% på tværs af 11 vesteuropæiske studier [9-19]. Et dansk studie rapporterede, at der i aldersgrupperne 67-79 år og +80 år var hhv. 19% og 13,3% mænd og 25,9% og 19,2% kvinder, der havde anvendt naturmedicin inden for de sidste 14 dage [19] (Tabel 2 i webudgaven). To andre danske studier [20, 21] rapporterede, at hhv. 63% og 66% af de ældre anvendte enten kosttilskud eller naturmedicin (Tabel 2 i webudgaven). Tre studier, der havde aldersopdelt deltagerne, konkluderede, at yngre ældre havde større tendens til at anvende naturmedicin end de ældste [11, 19, 22]. Eksempelvis fandt et studie, at 17,1% af de ældre på 80-89 år havde et forbrug af naturmedicin sammenlignet med 7,3% af de ældre over 90 år [11]. Overordnet var kvinder mere tilbøjelige til at anvende naturmedicin/alternativ medicin [9-12, 16-19, 21-23].
Hvilke typer naturmedicin anvendes?
Ti studier rapporterede, hvilke droger der hyppigst blev anvendt, men kun seks af studierne [14, 16, 20, 21, 24, 25] havde fokuseret specifikt på de ældres forbrug. Blandt de hyppigst anvendte droger, både blandt ældre og også generelt, var ginseng, baldrian, echinacea, ginkgo biloba, perikon, hvidløg og kæmpenatlysolie. Endvidere rapporterede fire af studierne forbrug af fiskeolie [20, 21, 24, 25], og heraf var to danske.
Hvor meget ved lægen om patienternes forbrug?
Syv ud af de 17 inkluderede studier havde undersøgt, hvor meget lægen vidste om patienternes brug af alternativ medicin. Disse undersøgelser viser samstemmende, at en betydelig del af patienternes forbrug af naturmedicin ikke er kendt af den behandlende læge i hverken primær eller sekundær sektor.
Interaktioner
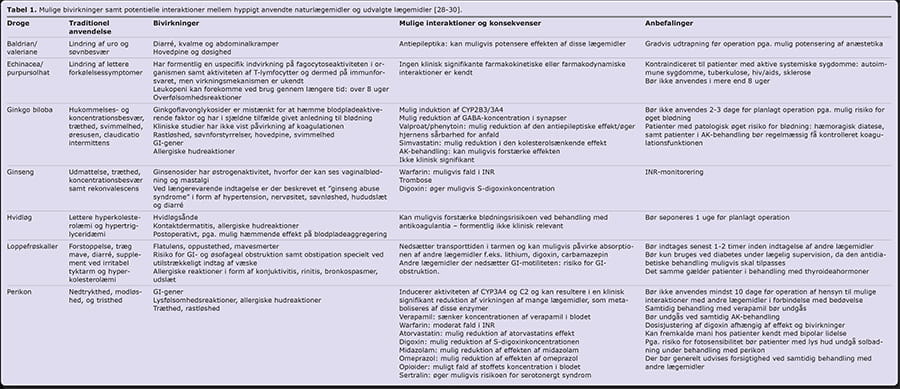
Det er vigtigt at være opmærksom på et muligt forbrug af håndkøbsmedicin, inklusive naturmedicin, hos ældre patienter pga. hyppig polyfarmaci og dermed risiko for interaktioner (se Tabel 1).
En oversigtsartikel om den kliniske evidens vedrørende interaktioner mellem natur- og konventionel medicin påpeger, at mange af de rapporterede interaktioner mellem natur- og konventionel medicin havde en begrænset klinisk signifikans. Få droger kan være skyld i interaktioner, der potentielt kan skade patienterne [26]. Eksempelvis er perikon en kendt inducer af CYP3A4, som potentielt kan sænke effekten af mange lægemidler, hvilket giver særlig problemer med antivirale, immunsuppressive og anticancermidler [27]. Det frarådes at tage verapamil eller warfarin sammen med perikon, da begge er substrater for CYP3A4, og samtidig brug kan medføre interaktioner [28]. Desuden har store mængder af tranebærsaft sammen med warfarin vist sig at øge INR, hvilket øger risikoen for blødning [28].
Tabel 1. Mulige bivirkninger samt potentielle interaktioner mellem hyppigt anvendte naturlægemidler og udvalgte lægemidler (28-30)
Referencer
- Danmarks Statistik. 82.000 flere af ikke-vestlig herkomst i Danmark. www.dst.dk/nyt/21575 (5. mar 2017).
- Hajjar ER, Cafiero AC, Hanlon JT. Polypharmacy in elderly patients. Am J Geriatr Pharmacother 2007;5:345-51.
- Salive ME. Multimorbidity in older adults. Epidemiol Rev 2013;35:75-83.
- Sundhedsstyrelsen. Hvad er naturmedicin? https://www.srab.dk/naturmedicin/hvad-er-naturmedicin/ (19. jan 2018 ).
- National Center for Complementary and Integrative Health. Complementary, alternative, or integrative health: what’s in a name? https://nccih.nih.gov/health/integrative-health (3. mar 2018).
- Institute of Medicine (US) Committee on the Use of Complementary and Alternative Medicine by the American Public. Complementary and alternative medicine in the United States. www.ncbi.nlm.nih.gov/books/NBK83799/ (3.mar 2018).
- Lægemiddelstyrelsen. Markedsføringstilladelse til naturlægemidler. https://laegemiddelstyrelsen.dk/da/godkendelse/godkendelse-afmedicin/markedsfoeringstilladelse/ansoegning-ommarkedsfoeringstilladelse/markedsfoeringstilladelse-tilnaturlaegemidler/(19. jan 2018).
- Alamgir ANM. Therapeutic use of medicinal plants and their extracts: Volume1: Pharmacognosy. Springer, 2017.
- Al-Windi A, Elmfeldt D, Svärdsudd K. Determinants of drug utilisation in a Swedish municipality. Pharmacoepidemiol Drug Saf 2004;13:97-103.
- Al-Windi A. Predictors of herbal medicine use in a Swedish health practice. Pharmacoepidemiol Drug Saf 2004;13:489-96.
- Stjernberg L, Berglund J, Halling A. Age and gender effect on the use of herbal medicine products and food supplements among the elderly. Scand J Prim Health Care 2006;24:50-5.
- Djuv A, Nilsen OG, Steinsbekk A. The co-use of conventional drugs and herbs among patients in Norwegian general practice: a cross-sectional study. BMC Complement Altern Med 2013;13:295.
- Büssing A, Ostermann T, Heusser P et al. Usage of alternative medical systems, acupuncture, homeopathy and anthroposophic medicine, by older German adults. Zhong Xi Yi Jie He Xue Bao 2011;9:847-56.
- Schnabel K, Binting S, Witt CM et al. Use of complementary and alternative medicine by older adults – a cross-sectional survey. BMC Geriatr 2014;14:38.
- Franke AG, Heinrich I, Lieb K et al. The use of Ginkgo biloba in healthy elderly. Age (Dordr) 2014;36:435-44.
- Dello Buono M, Urciuoli O, Marietta P et al. Alternative medicine in a sample of 655 community-dwelling elderly. J Psychosom Res 2001;50:147-54.
- Pugi A, Gallo E, Vannacci A et al. Herbal remedies in hospital setting: an Italian explorative survey among physicians and patients on knowledge and use. Intern Emerg Med 2011;6:575-6.
- Skinner CM, Rangasami J. Preoperative use of herbal medicines: a patient survey. Br J Anaesth 2002;89:792-5.
- 19. Nielsen MW, Hansen EH, Rasmussen NK. Use of natural medicines in the Danish population: a national crosssectional survey. Ann Pharmacother 2005;39:1534-8.
- Glintborg B, Andersen SE, Spang-Hanssen E et al. Disregarded use of herbal medical products and dietary supplements among surgical and medical patients as estimated by home inspection and interview. Pharmacoepidemiol Drug Saf 2005;14:639-45.
- Olesen C, Harbig P, Barat I et al. Absence of ‘over-the-counter’ medicinal products in on-line prescription records: a risk factor of overlooking interactions in the elderly. Pharmacoepidemiol Drug Saf
2013;22:145-50. - Thomas KJ, Nicholl JP, Coleman P. Use and expenditure on complementary medicine in England: a population based survey. Complement Ther Med 2001;9:2-11.
- Shakeel M, Bruce J, Jehan S et al. Use of complementary and alternative medicine by patients admitted to a surgical unit in Scotland. Ann R Coll Surg Engl 2008;90:571-6.
- Ramsay NA, Kenny MW, Davies G et al. Complimentary and alternative medicine use among patients starting warfarin. Br J Haematol 2005;130:777-80.
- Canter PH, Ernst E. Herbal supplement use by persons aged over 50 years in Britain: frequently used herbs, concomitant use of herbs, nutritional supplements and prescription drugs, rate of informing doctors and potential for negative interactions. Drugs Aging 2004;21:597-605.
- Izzo AA. Interactions between herbs and conventional drugs: overview of the clinical data. Med Princ Pract 2012;21:404-28.
- Whitten DL, Myers SP, Hawrelak JA et al. The effect of St John’s wort extracts on CYP3A: a systematic review of prospective clinical trials. Br J Clin Pharmacol 2006;62:512-26.
- Lægemiddelstyrelsen. Interaktionsdatabasen. www.interaktionsdatabasen.dk (18. feb 2017).
- Lægemiddelstyrelsen. Produktresuméer. www.produktresume.dk/ (10. feb 2018).
- ProMedicin. http://pro.medicin.dk (18.jun 2017).