Børneastma
Rationel farmakoterapi nr. 10, 2015
Månedsbladet opdateres ikke efter udgivelsen. Indholdet afspejler den aktuelle evidens på udgivelsestidspunktet.
Af Lone Agertoft
H.C. Andersen Børnehospital, Odense
Astma er den hyppigste kroniske sygdom hos børn og unge i den vestlige verden med forekomst op til 10 % i 15-års-alderen (1). Selvrapporteret har 20 % af 5-årige aktuelle astmasymptomer, og 38 % har på et tidspunkt haft det (2), men astmadiagnosen er mindre sikker i denne aldersgruppe. Nogle undersøgelser tyder på, at der stadig forekommer en ikke ubetydelig grad af over- og underdiagnosticering og –behandling (3,4).
Astma er en heterogen og multifaktoriel sygdom med betydelige aldersforskelle både med hensyn til årsager, mekanismer, diagnostik, behandlingsmuligheder og prognose. Hos småbørn er astmasymptomer oftest udløst af luftvejsinfektioner, men småbørn med svære/vedvarende symptomer kan også have allergi. Større børn med vedvarende astma har ofte allergi som medvirkende faktor. I alle aldersgrupper er luftvejsinfektioner den hyppigste årsag til forværringer.
Astma er således en hyppig kronisk sygdom, der skal behandles effektivt for at reducere risikoen for tab af lungefunktion og progression af sygdommen, reducere sygelighed og sygefravær for børn og forældre og sikre normal trivsel, udvikling og aktivitetsniveau.
I 2015 publicerede Rådet for Anvendelse af Dyr Sygehusmedicin (RADS) en behandlingsvejledning vedrørende evidensbaseret farmakologisk behandling af børn og unge med astma (5-9). Følgende anbefalinger er i overensstemmelse med anbefalingerne fra RADS.
Symptomer/diagnostik
Astma karakteriseres af varierende grad af hyperreagerende luftveje med anfaldsvis åndenød, pibende/hvæsende vejrtrækning og hoste spontant ved fysisk aktivitet eller ved udsættelse for luftvejsirriterende stoffer, fx røg og luftbårne allergener, samt infektioner. Endvidere kan der være nedsat aktivitetsniveau eller vedvarende hoste, hvorimod monosymptomatisk hoste sjældent er astma. Desuden skal differentialdiagnoser overvejes.
Allergiudredning
Alle børn med vedvarende behandlingskrævende astmasymptomer bør – uanset alder – have foretaget en allergiudredning med priktest og/eller allergenspecifik IgE. Der er ingen nedre aldersgrænse for allergitestning, men man bør vurdere, hvilke allergener det er relevant at teste for. Dette gælder specielt for små børn, hvor en reaktion på en hudpriktest ofte er mindre. Ved allergisk astma drejer det sig oftest om indendørs inhalationsallergener, især husstøvmider og pelsdyr, men det kan også være udendørsallergener som pollen, især hvis der samtidig er allergisk rhinit.
Mindre børn med infektionsudløste symptomer skal ikke allergiudredes.
Non-farmakologisk behandling
Miljøsanering
Eksposition for allergener og irritanter skal vurderes, og børn med allergi bør så vidt muligt undgå daglig kontakt med allergener, som de er påvist allergiske over for. Allergener kan påvises i hjemmet længe efter, at pelsdyret er væk.
Husstøvmider findes primært i sovemiljøet, dvs. madras, dyne, hovedpude, rullemadras og sovedyr, men også i gulvtæppe, især tæt på sengen.
Pollen vil i sæsonen være til stede overalt, og eksponering kan kun delvist reduceres.
Børn med astma bør ikke ryge eller eksponeres for daglig passiv rygning, og andre mulige irritanter bør undgås.
Inhalationsmetode
Valg af inhalationsdevice foretages ud fra en vurdering af barnets alder og udvikling for at sikre, at korrekt inhalationsteknik kan opnås (10). Man skal være opmærksom på, at børns evne til at kooperere og inhalere reduceres i forbindelse med akut sygdom. For at opnå bedst mulig adhærence bør patientens og forældrenes præferencer vedrørende valg af device indgå, og der bør sikres korrekt inhalationsteknik med det pågældende device (11). Der er desuden behov for at træne inhalationsteknik jævnligt (11,12), og anvendelse af samme slags device til alle patientens inhalationspræparater forbedrer muligheden for at opnå en god inhalationsteknik (13).
Førskolebørn kan ikke bruge spray uden spacer, og hos småbørn skal der tillige anvendes en tætsluttende ansigtsmaske (14). Sprayen rystes, hvorefter der affyres et pust i spaceren ad gangen, og barnet tager umiddelbart efter 6 rolige vejrtrækninger (tidal ånding) (15). Når barnet kan bide om mundstykket, og samtidigt holde læberne tæt lukket omkring spacerens mundstykke, kan masken fjernes.
Skolebørn kan, afhængigt af alder, evner og individuel træning, anvende pulverinhalatorer og åndedrætsaktiverede inhalationsaerosoler (16). Familierne skal instrueres i rengøring og vedligeholdelse af spacer/inhalator.
Farmakologisk behandling
Det er nødvendigt at tilpasse behandlingen og forløbet individuelt for at opnå så optimalt et resultat som muligt. Inhaleret medicin foretrækkes, da præparatet deponeres direkte i lungerne, og der opnås den bedste terapeutiske effekt med færrest systemiske bivirkninger. Næsten 2/3 af børn med astma har også »høfeber« med nasal obstruktion, hvorfor effektiv behandling af samtidig rhinit er væsentlig for at opnå god astmakontrol.
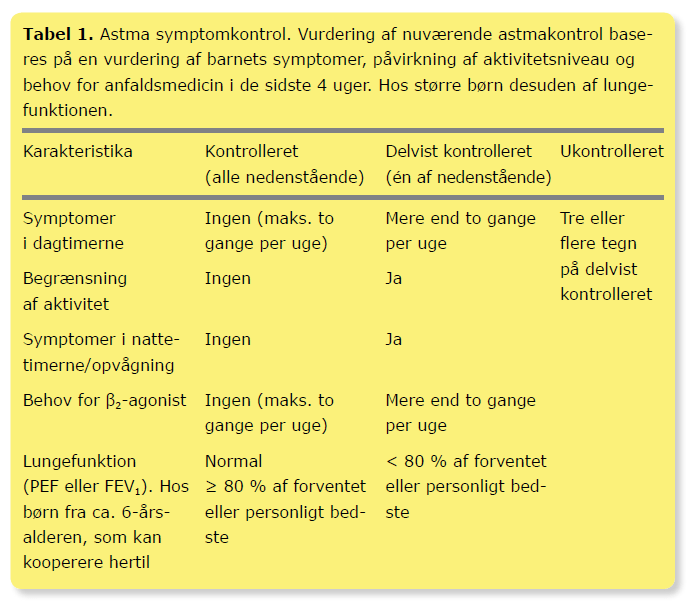
Sværhedsgraden af astma er meget varierende, både intra- og interindividuelt. Nogle børn har behov for daglig forbyggende behandling, mens andre vil kunne klare sig alene med anfaldsmedicin. Udredning, diagnostik og vurdering af sværhedsgrad er afgørende for behandlingen. Behandlingsbehovet kan vurderes ved en vurdering af graden af kontrol med symptomer og lungefunktion over de sidste 4 uger (Tabel 1). Ved astmasymptomer om dagen mere end 2 gange om ugen, behov for anfaldsmedicin mere end 2 gange om ugen eller symptomer om natten er der indikation for forebyggende behandling. Til daglig forebyggende behandling er inhalationssteroider (ICS) førstevalgspræparat. Behandling med ICS reducerer hyppig-heden af alvorlige eksacerbationer, forbruget af anden anti-astmatisk behandling og forbedrer lungefunktionen (17-19).
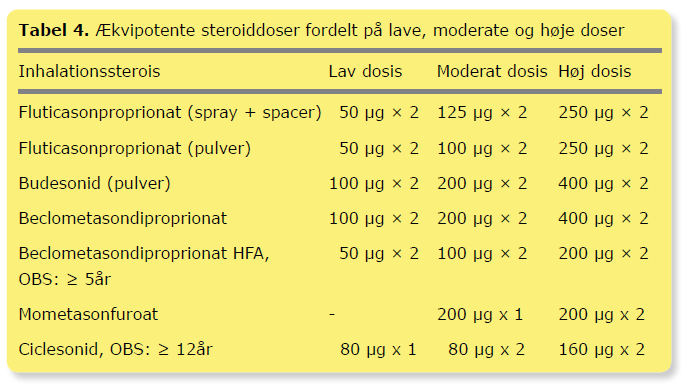
Som udgangspunkt behandles initialt med inhaleret korttidsvirkende β2-agonist dvs. i behandlingsalgoritmen svarende til trin 1 (Tabel 2 og 3). Hvis dette ikke medfører kontrol, øges til trin 2 eller 3 afhængigt af symptomernes sværhedsgrad. Ved svære/hyppige symptomer påbegyndes behandling med ICS, når diagnosen er sandsynliggjort. Ækvipotente ICS-doser er angivet i Tabel 4. Der er ikke evidens for bedre sygdomskontrol ved at starte med højdosis-ICS. Det anbefales, at behandlingseffekten vurderes højst 3 måneder efter behandlingsstart eller behandlingsændring og herefter med 3-6 måneders interval efter individuel vurdering. Når kontrol med astmasygdommen er opnået (Tabel 3), titreres ICS-dosis ned til laveste effektive dosis, hvor astmasymptomerne fortsat er under kontrol, og lungefunktionsniveauet hos de større børn også opretholdes. Hvis kontrol ikke opnås efter 2-3 måneders behandling, bør adhærence, inhalationsteknik, provokerende faktorer i barnets miljø (fx tobaksrøg) og evt. komorbiditet med allergisk rhinit vurderes, ligesom diagnosen skal revurderes. Dosis af ICS kan – afhængig af sværhedsgrad – øges eller reduceres gradvist med f.eks. 25-50 % ad gangen mod næste behandlingstrin. Hos alle børn, der påbegynder behandling med ICS, skal behandlingen betragtes som et behandlingsforsøg, og effekt og diagnose skal revurderes efter 2-3 måneder.
Hos større børn kan dosisreduktion overvejes efter 3-6 måneders god astmakontrol og stabil lungefunktion; ved velkontrolleret astma på trin 2, dvs. lavdosis-ICS i minimum 6-12 måneder, kan behandlingen seponeres. Hos småbørn med infektionsudløst astma kan dosisreduktion eller seponering forsøges efter 2-3 måneders god astmakontrol.
Ved utilstrækkelig effekt af den aftalte dosis ICS – trods god adhærence – kan der forsøgsvis suppleres med leukotrien-receptorantagonist (LTRA) eller langtidsvirkende β2-agonist (LABA) fremfor at øge ICS-dosis. Hos større børn (> 6 år) med delvist kontrolleret astma på moderat dosis ICS kan tillæg af LABA medføre bedre lungefunktion og nedsat behov for anfaldsmedicin; men det har ikke bedre effekt på antal eksacerbationer end dobbelt dosis ICS (20). LABA har ikke antiinflammatorisk effekt, og hvis LABA anvendes fast som monoterapi, er der risiko for, at det ikke opdages, hvis barnets astma ikke er kontrolleret – og der er dermed risiko for alvorlige eksacerbationer. Derfor anbefales LABA aldrig som fast monoterapi.
Tabletbehandling med LTRA er ikke så effektivt som lavdosis-ICS, men det kan anvendes som supplement til ICS. LTRA har ikke effekt hos alle, og det er ikke på forhånd muligt at vide, hvilke børn det virker på. Til mild astma hos småbørn er der vist nogen effekt af LTRA på kontrol af symptomer og viralt inducerede eksacerbationer (21,22).
Såvel LABA som korttidsvirkende β2-agonist kan anvendes før fysisk aktivitet ved anstrengelsesudløste symptomer (23). LTRA kan også anvendes som supplement til ICS ved anstrengelsesudløste symptomer (24). Børn med symptomer ved fysisk aktivitet har oftest behov for fast forebyggende behandling med ICS.
Behandling med Anti-IgE (omalizumab, Xolair) er en specialistopgave. Anti-IgE kan anvendes som tillægsbehandling hos børn > 6 år med vedvarende svær allergisk astma. Anti-IgE er et humaniseret monoklonalt antistof, der binder til immunglobulin E. Det gives subkutant hver 2.-4 uge afhængigt af vægt og totalt IgE.
Allergenspecifik immunterapi (AIT) kan overvejes hos børn med mild til moderat allergisk astma, hvor eksposition for et klinisk relevant allergen ikke kan undgås, hvor der ikke er tilstrækkelig effekt af farmakologisk behandling inklusive ICS, og hvor der er dokumenteret klinisk effekt af det pågældende allergenekstrakt. Risikoen for svære allergiske bivirkninger skal indgå i overvejelserne. Det er sandsynligt, at anvendelse af AIT kan have effekt på både allergisk rhinit og astma hos de børn, hvor begge sygdomme optræder samtidigt.
Bivirkninger af inhalationssteroider
Behandling med ICS kan give hæshed, irritation eller svamp i mundslimhinden, og ved brug af ansigtsmaske kan huden omkring munden blive irriteret. Generne kan afhjælpes ved, at den eksponerede hud afvaskes efter inhalation for at fjerne steroidrester. Ydermere kan der før inhalationen lægges et »beskyttende« lag creme på huden, og efterfølgende fjernes cremen sammen med steroid rester. Man kan forsøge at reducere risikoen for gener i mundhule og svælg ved at børste tænder eller skylle mund efter inhalationen, men der er ingen sikker evidens herfor.
Alle ICS i moderat til høj dosis (Tabel 4) kan påvirke væksten, når behandlingen påbegyndes, men vækstreduktionen er ikke progredierende ved vedvarende behandling. Om den initiale vækstreduktion bibeholdes til sluthøjde er ikke undersøgt tilstrækkeligt, og de to eneste langtidsvækststudier viser modsatrettede resultater (26,27), idet det ene viser ingen og det andet gennemsnitligt 1,2 cm (maksimalt 1,9 cm) reduktion i sluthøjden. Vigtige faktorer for sluthøjde synes også at være højden ved ICS-behandlingens start samt pubertetsstadie, idet præpubertale børn vurderes mest følsomme (26). Det er også vigtigt at vide, at ikke-kontrolleret astma i sig selv kan hæmme væksten (28), og at børn med astma ofte, og uafhængigt af ICS-behandling, har en langsom vækst og forsinket pubertet, som indhentes senere.
Behandling med moderate doser ICS har ikke givet anledning til osteoporose eller øget risiko for fraktur, hvorimod kure med systemisk steroid påvirker knoglerne og øger frakturrisikoen (29,39).
Monitorering
Målet med behandling er symptomkontrol, normalt aktivitetsniveau, normal lungefunktion og minimal risiko for eksacerbationer og bivirkninger.
En forudsætning for, at en given behandling er effektiv, er, at den tages af patienten, og at den tages korrekt. Den hyppigste årsag til utilstrækkelig effekt af astmabehandling hos børn er, at barnet ikke får sin forebyggende ICS-behandling som aftalt, eller at inhalationsteknikken ikke er korrekt. Det er vist, at adhærence er en stærk prædiktor for langtids astmakontrol, og adhærence > 80 % er korreleret til den bedste grad af kontrol (31), samt at non-adhærence er associeret med flere akutte lægebesøg og hospitaliseringer (32).
Behandlingen af et barns astma er et samarbejde mellem barnet, forældrene og lægen og bør vurderes ved regelmæssige kliniske kontroller, hvor symptomer, behovet for β2-agonist, peak-flow og for større børn spirometri, fysisk aktivitetsniveau og behov for justering af behandlingen vurderes. Endvidere kontrolleres inhalationsteknikken ved alle kontroller, og minimum en gang årligt måles barnets højde.
Familierne bør have en skriftlig behandlingsplan og instrueres i, hvordan man skal forholde sig i tilfælde af akutte forværringer.
Ved svær/kompliceret astma eller tvivl om diagnosen bør der henvises til en børnelæge med specialviden om astma hos børn (se boks).

Referencer
(1) Thomsen SF, Ulrik CS, Kyvik KO, Larsen K, Skadhauge LR, Steffensen I, et al. The incidence of asthma in young adults. Chest 2005;Jun;127(6):1928-34.
(2) Hermann C, De Fine Olivarius N, Høst A, Begtrup K, Hollnagel H. Prevalence, severity and determinants of asthma in Danish five-year-olds. Acta Paediatr 2015;Oct;95(10):1182-90.
(3) Zilmer M, Steen NP, Zachariassen G, Duus T, Kristiansen B, Halken S. Prevalence of asthma and bronchial hyperreactivity in Danish Schoolchildren: no change over 10 years. Acta Pediatr 2011;Mar;100(3):385-9.
(4) Hoffmann-Petersen B, Høst A, Larsen KT, Bergstein KR, Thomsen ML, Braendholdt V, et al. Prevalence of IgE sensitization in Danish children with suspected asthma. Pediatr Allergy Immunol 2013;Dec;24(8):727-33.
(5) Rådet for anvendelse af Dyr Sygehusmedicin (RADS), fagudvalg for børneastma. http://www.regioner.dk/aktuelt/nyheder/2015/januar/ny+vejledning+for+behandling+af+børn+med+astma. 2015.
(6) Bønnelykke K, Pedersen S, Rubak I.M.S, Schiøtz O, Bisgaard H. Astma hos børn. Ugeskrift for Læger 2013;Aug 175/33:1863-7.
(7) From the Global Strategy for Asthma Management and Prevention, Global Initiative for Asthma (GINA). Available from http://www.ginaasthma.org/. 2014.
(8) BTS/SIGN British Guideline on the management of asthma. Available from: http://www.brit-thoracic.org.uk/. 2012.
(9) From the Global Strategy for Asthma Management and Prevention. Global strategy for the Diagnosis and Management of asthma in children 5 years and younger. Available from http://www.ginaasthma.org/. 2009.
(10) Haughney J, Price D, Barnes NC, Virchow JC, Roche N, Chrystyn H. Choosing inhaler devices for people with astma: current knowledge and outstanding research needs. Resp Med 2010;Sep;104(9):1237-45.
(11) Price D, Bosnic-Anticevich S, Briggs A, Chrystyn H, Rand C, Scheuch G, et al. Inhaler competance in asthma: common errors, barriers to use and recommended solutions. Resp Med 2013;Jan;107(1):37-46.
(12) Lavorini F, Usmani OS. Correct inhalation technique is critical in achieving good asthma control. Prim Care Respir J 2013;Dec;22(4):385-6.
(13) Van der Palen J, Kelin JJ, van Herwaarden CL, Zielhuis GA, Seydel ER. Multiple inhalers confuse asthma patients. Eur Respir J 1999;Nov;14(5):1034-7.
(14) Ditcham W, Murdzoska J, Zhang G, Roller C, von Hollen D, Nikander K, et al. Lung Deposition of 99mTc-Radiolabeled Albuterol Delivered through a pressurized Metered Dose Inhaler and Spacer with Facemask or Mouthpiece in Children with Asthma. J Aerosol Med Pulm Drug Deliv 2014;Aug;27(Suppl 1):S63-S75.
(15) Schultz A, Le Souef TJ, Venter A, Zhang G, Devadason SG, Le Souef PN. Aerosol inhalation from spacers and valved holding chambers requiers few tidal breaths for children. Pediatrics 2010;Dec;126(6):e1493-8.
(16) Basheti IA, Bosnic-Anticevich SZ, Armour CL, Reddel HK. Checklists for dry powder inhaler technique: a review and a recommandation. Respir Care 2014;Jul;59(7):1140-54.
(17) Castro-Rodriquez JA, Rodrigo GJ. Efficacy of inhaled corticosteroids in infants and preschoolers with recurrent wheezing and asthma: a systematic review with meta-analysis. Pediatrics 2009;Mar;123(3):e519-25.
(18) Busse WW, Pedersen S, Pauwels RA, Tan WC, Chen YZ, Lamm CJ, et al. The inhaled stroid treatment as regular therapy en early asthma (START) study 5-year follow-up: Effectiveness of early intervention with budesonide in mild persistent asthma. J Allergy Clin Immunol 2008;May;121(5):1167-74.
(19) Teper AM, Kofman CD. Treatment with inhaled corticosteroids improves pulmonary functionin children under 2 years old with risk factors for asthma. Curr Opin Allergy Clin Immunol 2006;Jun;6(3):152-4.
(20) Castro-RodriqueZ JA, Rodrigo GJ. A systematic review of long-term beta2-agonist versus higher doses of inhaled corticosteroids in asthma. Pediatrics 2012;Sep;130(3):e650-7.
(21) Bisgaard H, Zielen S, Garcia-Garcia ML, Johnston SL, Gilles L, Menten J, et al. Montelukast reduces asthma exacerbations in 2- to 5-year-old children with intermittent asthma. Am J Respir Crit Care Med 2005;Feb 15;171(4):315-22.
(22) Garcia-Garcia ML, Wahn U, Gilles L, Swem A, Tozzi CA, Polos P. Montelukast, compared with fluticasone, for control of asthma among 6- to 14-year-old patients with mild asthma: the MOSAIC study. Pediatrics 2015;Aug;116(2):360-9.
(23) Murray JJ, Waitkus-Edwards KR, Yancey SW. Evaluation of fluticasone propionate and fluticasone propionate/salmeterol combination on exercise in pediatric and adolescent patients with asthma. Open Respir Med J 2011;5:11-8.
(24) Duong M, Amin R, Baatjes AJ, Kritzinger F, Qi Y, Meghji Z, et al. The effect of montelukast, budesonide alone, and in combination on exercise-induced bronchoconstriction. J Allergy Clin Immunol 2012;Aug;130(2):535-9.
(25) Yousef E, Hossain J, Mannan S, Skorpinski E, McGeady S. Early intervention with high-dose inhaled corticosteroids for control og acute asthma exacerbations at home and improved outcomes: a randomized controlled trial. Allergy Asthma Proc 2012;Nov-Dec;33(6):508-13.
(26) Kelly HW, Sternberg AL, Lescher R, Fuhlbrigge AL, Williams P, Zeiger RS, et al. Effect of inhaled glucicorticoids in childhood on adult height. N Engl J Med 2012;Sep 6;367(10):904-12.
(27) Agertoft L, Pedersen S. Effect of long-term treatment with inhaled budesonide on adult height in children with asthma. N Engl J Med 2000;Oct 12;343(15):1064-9.
(28) Murray AB, Fraser BM, Hardwick GL, Pirie GE. Chronic asthma and growth failure in children. Lancet 1976;Jul 24;2(7989):197-8.
(29) Muley P, Shah M, Muley A. Safety of inhaled fluticasone propionate therapy for pediatric asthma a systematic review. Curr Drug Saf 2013;Jul;8(3):186-94.
(30) Vestergaard P, Rejnmark L, Mosekilde L. Fracture risk associated with systemic and topical corticosteroids. J Intern Med 2005;Apr;257(4):374-84.
(31) Klok T, Kaptein AA, Duiverman EJ, Brand PL. It´s the adherence, stupid (that determines asthma control in preschool children)! Eur Respir J 2014;Mar;43(3):783-91.
(32) McGrady ME, Hommel KA. Medication adherence and health care utilization in pediatric chronic illness: a systematic review. Pediatrics 2013;Oct;132(4):730-40.