Den gamle medicinbruger
Artikel fra Rationel Farmakoterapi 4, 2017
Lene Ørskov Reuther Geriatrisk/Ældremedicinsk afd. G, OUH
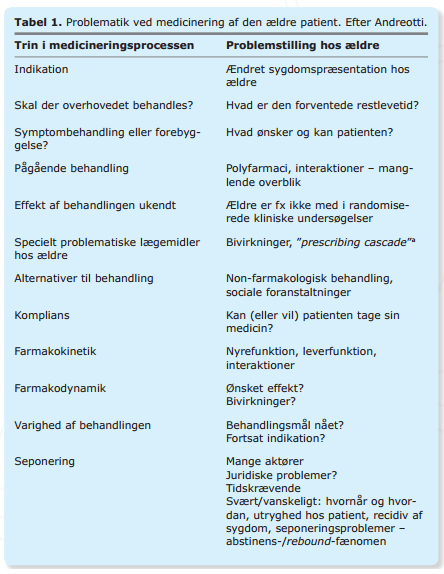
Som belyst på Institut for Rationel Farmakoterapis Stormøde, februar 2017, er medicineringen af den ældre patient, vanskelig lige fra overvejelse om behandlingsindikation til synlig effekt og evt. seponering (Tabel 1) (1). I denne artikel vil udvalgte områder blive gennemgået.
Viden om lægemidlers effekt hos ældre
Det er vist, at ældre sjældent medtages i de randomiserede undersøgelser, der er grundstenen i vurderingen af medicin (2). Det er primært yngre patienter, som inkluderes. Der synes ikke at være udsigt til, at ældre vil blive inkluderet i disse studier i større stil. Andre studiedesign må overvejes. Her tænkes bl.a. på observationelle studier, som bedre kan se på effekten hos multimedicinerede og multisyge patienter (3), eller ”pragmatic trials”, hvor studierne udføres som led i den daglige klinik (4). Disse studier kritiseres dog ofte for confounding.
Et andet problem er, at numerisk alder ofte i sig selv er et inklusions-kriterie, mens fysiologisk alder/funk-tionsniveau er langt mere relevant. Helt centralt er skrøbelighed (frailty), som beskrives ved bl.a. nedsat udholdenhed, styrke og reduceret fysiologisk funktion. Frailty siger mere om en ældres tilstand end alder (5), og burde ideelt set indgå i udvælgelseskriterierne.
Polyfarmaci
Pga. multisygdom vil den ældre ofte blive udsat for polyfarmaci. Således fik 60% af 75-årige på plejehjem i Danmark tre eller flere lægemidler (6), og mange mindst ti. Dette giver manglende overblik og viden om, hvad patienten får af medicin (7,8), om end Det Fælles Medicinkort, FMK, kan minimere dette problem. De mange lægemidler giver også et helt uoverskueligt net af interaktioner, hvor opslag i fx Interaktionsdatabasen vil resultere i en lang liste af mulige interaktioner – med varierende klinisk relevans.
De mange sygdomme fører til svær polyfarmaci, når guidelines for de enkelte tilstande følges slavisk. Her savnes der vejledning i, hvilke lægemidler der er de vigtigste, og hvilke der bedst kan undværes/seponeres.
Det kunne overvejes, om man ved udarbejdelse af guidelines og lignende bør forlange lister med fx »guld-, sølv- hhv. bronzepræparater« inden for de største sygdomsområder hos ældre som prioriteringsværktøjer til lægen, når der vælges mellem flere for sygdommene indicerede lægemidler. Dette kunne hensigtsmæssigt ske i et samarbejde mellem de lægevidenskabelige selskaber og kliniske farmakologer ved udarbejdelse af behandlingsvejledninger og -guidelines.
Farmakokinetik
Den vigtigste faktor for ændret kinetik er aldersbetinget reduceret nyrefunktion, der ses med stor interindividuel variation (9), mens ændringer i absorption, proteinbinding, fedt-/vandfaser i kroppen ikke giver betydningsfulde ændringer i kinetikken hos ældre (10). Dette har naturligvis størst betydning for primært renalt eliminerede lægemidler, fx digoxin, NOAK og visse antidiabetika etc. Ved tvivl tilrådes det at slå op i stoffets produktresumé, hvorvidt nedsat nyrefunktion har betydning for dosering. Den langsomme reduktion af nyrefunktion over tid betyder, at man ikke altid opdager, at nyrefunktionen er blevet reduceret med risiko for overdosering og evt. forgiftning. Derfor bør nyrefunktion måles ved årskontrollerne ved kroniske lidelser, både i primær og sekundær sektor.
Leverfunktionen aftager i mindre grad med alderen, og den hepatiske elimination forbliver ifølge nogle forfattere uændret med alderen (10). Andre anfører, at aktiviteten af de forskellige cytochrom P450-enzymer reduceres med alderen med langsommere elimination til følge (1). Ved tvivl om dosering af et hepatisk elimineret lægemiddel anbefales dette undersøgt ved hjælp af produktresuméet, som nemt kan tilgås via fx promedicin.dk.
Farmakodynamik
Lægemidler kan virke kraftigere på den ældre patient. Det kan være resultatet af den ændrede kinetik og dermed højere medicinkoncentration i blodet eller et resultat af en kraftigere interaktion mellem medicin og receptor – forhold som ikke kan måles i den daglige klinik (11). Der anføres ofte større effekt af CNS-aktive lægemidler hos den ældre (12), således at der kræves tættere klinisk kontrol og måske dosisreduktion, fx af morfin.
Non-farmakologisk behandling
Non-farmakologisk behandling bør altid indtænkes: Kan fysioterapi bruges i stedet for analgetika ved bevægeapparatsmerter? Kan sociale foranstaltninger hjælpe den ensomme skrøbelige triste ældre som alternativ til antidepressiv behandling (13)? Kan delir behandles med skærmning, fast vagt, ro m.m. i stedet for fx haloperidol (14)?
Komplians
Komplians hos ældre, som selv tager deres medicin, er varierende (15): Nogle ældre vil være mere autoritetstro og dermed have bedre komplians end gennemsnittet. Omvendt ved kognitiv svækkelse, hvor mistro eller tvivl om behandlingens nødvendighed samt vanskelighed ved at huske at tage medicinen giver dårlig komplians (16). Også specielle medicineringsprocedurer (fx fastende indtag af osteoporosemedicin eller diverse inhalations- devices) kan nedsætte komplians. Endelig kan misforståelser, manglende overblik og usikkerhed om medicinens navn/indhold spille ind. Disse forhold kan synes trivielle, men de kompromitterer ofte effekten af behandlingen og øger risikoen for utilsigtede hændelser, herunder bivirkninger. Derfor er der ofte behov for hjælp fra hjemmepleje, evt. brug af dosisdispensering hos den stabilt medicinerede patient etc.
Specielt problematiske lægemidler hos ældre
Specielt problematiske lægemidler hos ældre Der findes talrige lister over problematiske lægemidler hos ældre, hvor seponering bør overvejes (17), behandling ikke påbegyndes eller forsigtighed udvises (11). Men mange af de anførte lægemidler er nogle af de mest anvendte og ofte uundværlige ved behandling af ældre. Fx advares ofte mod digoxin, som på den anden side ofte vil være at foretrække til frekvensregulering ved atrieflimren hos ældre som alternativ til β-blokker, der kan give ortostatisk hypotention og mulige psykiske bivirkninger (18). Tilsvarende gælder opioider og andre stærkt virkende analgetika, hvor svært livskvalitetsnedsættende smerter må opvejes mod de kendte opioidbivirkninger. Det generelle råd vil være: »start forsigtigt og følg op«.
Specielt skal her tre lægemiddelgrupper fremhæves:
NSAID
Aldersrelateret øget risiko for gastrointestinal blødning samt kardielle bivirkninger, begge evt. med dødelig udgang (19). Af særlig betydning for den ældre patient ses væskeretention og påvirket nyrefunktion. Som udgangspunkt bør den ældre patient ikke behandles med NSAID.
Antikolinergika (antispasmolytika, bronkodilaterende antikolinergika, visse antiarytmika, antihistaminer, tricykliske antidepressiva, antiparkinsonmidler, muskelrelaksantia, antipsykotika m.m.)
Der advares ofte mod bivirkninger ved disse lægemidler i form af CNS-påvirkning, fald, obstipation, urinretention og øget dødelighed (20). Studierne er inkonklusive, hvad angår mortalitet og hospitalsindlæggelse (20,21). For mange af disse lægemidler er der god indikation hos ældre patienter. Der må så fokuseres på at bruge dem under observation for effekt og bivirkninger samt instruktion af lægemiddelhåndterende personale.
Psykofarmaka
Indtænk altid, at behandling med psykofarmaka er en af de vigtigste risikofaktorer for fald hos ældre (22), og seponering er en af de mest effektive in- terventioner mod fald. Benzodiazepiner giver eller forværrer kognitiv svækkelse hos mange ældre (23). Det er velkendt, at afhængigheden er stor, udtrapning vanskelig, og mange ældre mener, at de ikke kan undvære deres »sove-/beroligende pille« (24). Imidlertid må man også være opmærksom på, at benzodiazepiner kan være indicerede til kortvarig behandling af angst, men at nyere antidepressiva, fx mirtazepin, ofte har en »bedre« bivirkningsprofil, og at non-farmakologiske tiltag bør være førstevalg.
Behandlingsvarighed
Når en behandling påbegyndes, skal der altid tages stilling til behandlingsmål og -varighed. Dette gælder specielt for ældre i behandling med flere lægemidler. • at få større viden om medicins virkning på den ældre patient • at udbrede brugen af klinisk farmakologiske principper, når den ældre patient medicineres • at øge lægemiddelhåndterende aktørers (læger, plejepersoner m.m.) kommunikation med både patient og hinanden om patientens medicinering, således at uhensigtsmæssig medicinering/irrationel polyfarmaci ikke opstårMedicingennemgang
Som sundhedsprofessionel involveret i den medicinske behandling af ældre vil man ofte have behov for at skabe overblik over alle forhold omkring medicineringen fx komplians, ajourført medicinliste, korrekt dosering etc.
Mange studier har vist den potentielt skadelige effekt af medicin hos ældre. Således tilskrives ca. 10% af akutte medicinske indlæggelser medicin (25). Patienter falder pga. psykofarmaka (22), og ældre patienter med megen medicin har større risiko for død (26), for blot at nævne nogle effekter.
Et dansk registerstudie viste, at kun godt en tredjedel af de foretagne ændringer under indlæggelse på geriatrisk afdeling blev fortsat i almen praksis efter udskrivelse (27). Efterfølgende diskussion med praktiserende læger af resultatet gav mange forklaringer, men manglende rettidig og god information til den praktiserende læge var en vigtig faktor.
Intuitivt har en grundig medicingennemgang (MGG) været set som løsningen på ovenstående problemer og er i stor stil blevet introduceret på danske sygehuse og i primærsektoren.
Men trods talrige forsøg med forskellige design har man ikke fundet overbevisende effekt af MGG på hårde effektmål, herunder nedsat mortalitet og morbiditet, færre indlæggelser osv (28,29). Der er dog en vis effekt på parametre som reduktion i hhv. antal fald, antal lægemidler og antal skadestuebesøg. MGG synes at have sin berettigelse som værktøj til at sikre, at patienten får netop de lægemidler, der i et samarbejde mellem læge og patient er fundet indikation og mulighed for, herunder at diskutere mulighed for aktivt at fravælge i øvrigt indicerede lægemidler, hvis patientens tilstand og ønsker kræver dette.
Men problemet bør basalt angribes fra den modsatte ende: inden polyfarmaci overhovedet opstår som resultatet af (ofte mange) lægers behandling. Tværfaglig og tværsektoriel kommunikation om ændringer af patientens medicin er en nødvendighed (»den gode epikrise«, ajourført FMK m.m.), ligesom respekt for hinandens ordinationer (valg og fravalg) tværsektorielt er væsentlig. Endelig er samtalen med patienten (og evt. pårørende og plejepersoner) om den for patienten rigtige medicinliste vigtig.
Indtil da må der laves medicingennemgange med »sund fornuft« (30) og med de redskaber og hjælpemidler, der findes (31).
Konklusion
-
at få større viden om medicins virkning på den ældre patient
-
at udbrede brugen af klinisk farmakologiske principper, når den ældre patient medicineres
-
at øge lægemiddelhåndterende aktørers (læger, plejepersoner m.m.) kommunikation med både patient og hinanden om patientens medicinering, således at uhensigtsmæssig medicinering/irrationel polyfarmaci ikke opstår
-
at muligheder for seponering af behandling altid adresseres i behandlingsvejledninger og -guidelines.
Korrespondance
Litteraturreferencer
- Andreotti F, Rocca B, Husted S et al. ESC Thrombosis Working Group. Antithrombotic therapy in the elderly: expert position paper of the European Society of Cardiology Working Group on Thrombosis. Eur Heart J. 2015 Dec 7;36:3238-49.
- Kennedy-Martin T, Curtis 2, Faries D et al. A literature review on the representativeness of randomized controlled trial samples and implications for the external validity of trial results. Trials. 2015 Nov 3;16:495.
- Tinetti ME, McAvay G, Trentalange M et al. Association between guideline recommended drugs and death in older adults with multiple chronic conditions: population based cohort study. BMJ. 2015 Oct 2;351:h4984. doi: 10.1136/bmj.h4984.
- Bjerre E, Brasso K, Midtgaard J. [Pragmatic trials are important to medical research]. Ugeskr Laeger. 2015 Jul 27;177(31).
- Gordon AL1, Masud T, Gladman JR. Now that we have a definition for physical frailty, what shape should frailty medicine take? Age Ageing. 2014 Jan;43:8-9
- Lægehåndogen 2014
- Glintborg B, Andersen SE, Dalhoff K. Insufficient communication about medication use at the interface between hospital and primary care. Qual Saf Health Care 2007;16(1):34–39
- Rabøl R, Arrøe GR, Folke F et al. Disagreement between physicians' medication records and information given by patients. Ugeskr Laeger. 2006 Mar 27;168:1307-10. <
- http://www.irf.dk/dk/publikationer/rationel_farmakoterapi/maanedsblad/2012/laegemiddeldosering_ved_nedsat_nyrefunktion_og_anvendelse_af_egfr.htm (jan. 2017)
- Rosholm JU, Skjelbo E. Medicin til ældre. Medicinering af ældre. I: Brøsen K, Kampman JP red. Basal og klinisk farmakologi. FADL’s forlag 2014.
- Corsonello A1, Pedone C, Incalzi RA. Age-related pharmacokinetic and pharmacodynamic changes and related risk of adverse drug reactions. Curr Med Chem. 2010;17:571-84.
- Mukhtar O, Jackson SH .Drug therapies in older adults (part 1).Clin Med (Lond). 2015 Feb;15:47-53.
- Hansen DG, Rosholm JU , Gichangi A. Increased use of antidepressants at the end of life: population-based study among people aged 65 years and above. Age Ageing 2007 36: 449-454
- https://www.sst.dk/da/udgivelser/2016/~/media/9B627A494BCC4A8F804BE7BDDC3421BA.ashx (jan. 2017)
- Marcum ZA, Hanlon JT, Murray MD. Improving Medication Adherence and Health Outcomes in Older Adults: An Evidence-Based Review of Randomized Controlled Trials. Drugs Aging. 2017 Jan 10. doi: 10.1007/s40266-016-0433-7. [Epub ahead of print]
- Elliott RA, Goeman D, Beanland C et al. Ability of older people with dementia or cognitive impairment to manage medicine regimens: a narrative review. Curr Clin Pharmacol. 2015;10:213-21.
- http://www.irf.dk/download/medicingennemgang/forslag_til_seponering_af_laegemidler_hos_voksne.pdf
- Medicin.dk
- http://www.sst.dk//-/media/Udgivelser/2013/NSAID-Non-steroide-antiinflammatoriske-lægemidler,-d-,-Opgørelse-af-forbrug-indberettede-bivirkninger.ashx (jan. 2017)
- Cardwell K, Hughes CM, Ryan C. The Association Between Anticholinergic Medication Burden and Health Related Outcomes in the 'Oldest Old': A Systematic Review of the Literature. Drugs Aging. 2015 Oct;32:835-48
- Collamati A, Martone AM, Poscia A et al. Anticholinergic drugs and negative outcomes in the older population: from biological plausibility to clinical evidence. Aging Clin Exp Res. 2016 Feb;28:25-35.
- Woolcott JC, Richardson KJ, Wiens MOet al. Meta-analysis of the impact of 9 medication classes on falls in elderly persons. Arch Intern Med. 2009 Nov 23;169:1952-60.
- Airagnes G, Pelissolo A, Lavallée M et al. Benzodiazepine Misuse in the Elderly: Risk Factors, Consequences, and Management. Curr Psychiatry Rep. 2016 Oct;18:89.
- http://www.irf.dk/dk/publikationer/rationel_farmakoterapi/maanedsblad/2015/nedtrapning-af-benzodiazepiner-8722-haandtering-i-klinisk-praksis.htm (jan. 2017)
- Hallas J, Gram LF, Grodum E et al. Drug related admissions to medical wards: a population based survey. Br J Clin Pharmacol. 1992 Jan;3361-8
- Wester K1, Jönsson AK, Spigset O et al. Incidence of fatal adverse drug reactions: a population based study. Br J Clin Pharmacol. 2008 Apr;65:573-9.
- Larsen MD, Rosholm JU, Hallas J. The influence of comprehensive geriatric assessment on drug therapy in elderly patients. Eur J Clin Pharmacol. 2014 Feb;70:233-9
- Christensen M, Lundh A. Medication review in hospitalised patients to reduce morbidity and mortality. Cochrane Database Syst Rev. 2016 Feb 20;2:CD008986.
- Clyne B, Fitzgerald C, Quinlan A et al. Interventions to Address Potentially Inappropriate Prescribing in Community-Dwelling Older Adults: A Systematic Review of Randomized Controlled Trials J Am Geriatr Soc 64:1210–1222, 2016
- Tomsen DV .Medicingennemgang – kun en del af svaret. Ugeskr Laeger. 2016 Nov 14;178.
- http://www.irf.dk/dk/publikationer/rationel_farmakoterapi/maanedsblad/2014/seponering_af_medicin.htm (jan. 2017)